ホーム > トピック・関連情報 > プレスリリース > 血圧のような複雑な遺伝的性質の人種差の仕組みを解明
血圧のような複雑な遺伝的性質の人種差の仕組みを解明
2018年12月12日
国立国際医療研究センター
米国科学誌『Nature Communications』掲載
Interethnic analyses of blood pressure loci in populations of East Asian and European descent
(要旨)
国立国際医療研究センター研究所 遺伝子診断治療開発研究部 加藤 規弘 部長らのグループは、理化学研究所、大阪大学、名古屋大学、京都大学、島根大学、愛媛大学、愛知学院大学等の研究者とともに、International Genomics of Blood Pressure (iGEN-BP) Consortiumにおける多施設国際共同研究として、人種横断的な大規模ゲノムワイド関連解析(GWAS※1)を行い、その研究成果が国際的科学誌『Nature Communications』に掲載されました。
今回の研究の主な成果は以下の点です。
- 血圧(高血圧)という、世界的にみて最もありふれた、そして重要な生活習慣病指標(疾患)に関して、人種横断的な大規模ゲノムワイド関連解析を実施し、新規のもの19カ所を含む、計234遺伝子座を同定・確認した。
- 血圧(高血圧)との関連を示す遺伝子座のDNAバリアント(一塩基多型(SNP)など)には人種差があり、その仕組みとして「祖先特有バリアントの遺伝的関連モデル」を新たに提唱するとともに自然選択の影響を示した。
- 遺伝的効果を東アジア人と欧州人の間で比較した場合、ゲノム全域にわたる相関関係は比較的大きいものの、遺伝子座単位では、5%以上の遺伝子座において有意な人種差が見られることが実証された。
本研究の意義として、①これまで漠然ととらえられていた、血圧のような複雑な遺伝的性質の人種差について、その発生機序の一部を明らかにし、影響の度合いを実証したことで、より精密な生活習慣病の予測・診断法や予防法の開発につながると期待される点、及び②集団・人種横断的なゲノム解析においては、集団・人種どうしの、自然選択に関わるような環境要因の潜在的な違いにも留意する必要があると裏付けられた点が挙げられます。
研究の背景
高血圧の発症に遺伝が関与することは古くから知られており、一般集団中の血圧値分散の30-50%が遺伝要因によって規定されると推測されています。高血圧のうち、明らかな原因疾患があって生じるもの(二次性高血圧)は1割にも満たず、多くが原因不明な本態性高血圧です。本態性高血圧症は数多くの遺伝子と様々な生活習慣とが複雑に絡み合って発症するようですが、親から受け継ぐ“高血圧体質”の基盤を成す感受性遺伝子の実体は長らく不明でした。そこで2009年以降、人種単位で大規模コンソーシアムが組織されて、GWAS及びそのメタアナリシスの手法で、血圧(高血圧)の遺伝子座を同定しようとする試みが精力的に為されてきました。その結果、これまでに、合わせて200を超える血圧関連遺伝子座が、欧州人を中心に同定されてきました。東アジア人では高血圧の罹患率が高く、脳卒中の発症リスクを高めています。こうした臨床的特徴の人種差には、生活習慣の違いとともに遺伝要因の違いも少なからず影響すると考えられてきましたが、その詳細は不明でした。
研究の内容
本研究では、東アジア人に特異的及び/または人種横断的な血圧関連遺伝子を見出すため、最初に東アジア人13万人余の集団で、さらに欧州人と合わせた約29万人の集団での二段階スクリーニング法によるGWASメタアナリシスを行いました。その結果、ゲノムワイドな有意水準※2を満たす遺伝子座を55カ所同定し、加えて、同水準には達しないものの、既報の179遺伝子座で有意な関連を追試確認しました。従って、今回の研究で高血圧関連遺伝子座といえるものは合計234カ所となります。このうちの19カ所は以前に報告されておらず新規の高血圧関連遺伝子座です。
GWASの手法で同定・確認される高血圧関連遺伝子座のうち、どれくらいが人種特異的なものか、その特異性は如何に生じているのかが検証すべき課題です。本研究の東アジア人と欧州人のGWASデータは各々10万人を超えており、今回はじめて、遺伝的効果の人種間比較をゲノム全域にわたって相応の統計学的検出力で行えるサンプル規模となりました。そして我々は、集団遺伝学※3の解析手法を用いて、大きく、DNAバリアントの由来・構成の違いと自然選択の影響を検討しました。
SNPどうしには一定の‘連動性ないし近縁関係’(連鎖不平衡といいます)が存在し、このパターンが人種によって少なからず異なることはこれまでも知られていました。その人種差を利用して疾患感受性遺伝子座の精密マッピング※4なども行われています。連鎖不平衡は、対象集団の祖先が持っていた特定のハプロタイプ※5が保存されているために生じる場合が多いのですが、自然選択の影響によって大きな染色体領域で連鎖不平衡が生じている場合もあります。生物の進化を説明する自然選択説では、自然環境が、生物に無作為に生じる変異(突然変異)を選別して、進化に方向性を与えていると考えられています。この際、突然変異が環境に適応し「有利な」ものであれば正の選択が、「不利な」ものであれば負の選択が働きます。自然選択と生活習慣病との関係性について50年以上前に提唱された仮説として倹約遺伝子仮説※6があります。これは、近代化に伴って肥満や2型糖尿病が急増した原因を説明するために提唱されたものです。遠い昔には、飢餓を生き延びる上で有利な倹約遺伝子(脂肪を蓄積しエネルギーを貯め込む遺伝子)のタイプが選択されましたが、飽食の現代においては、それが肥満や2型糖尿病の増加を招いてしまっているという仮説です。過去数十年間、様々な検証が試みられましたが、この仮説を裏付ける確定的な証拠はまだ得られていません。
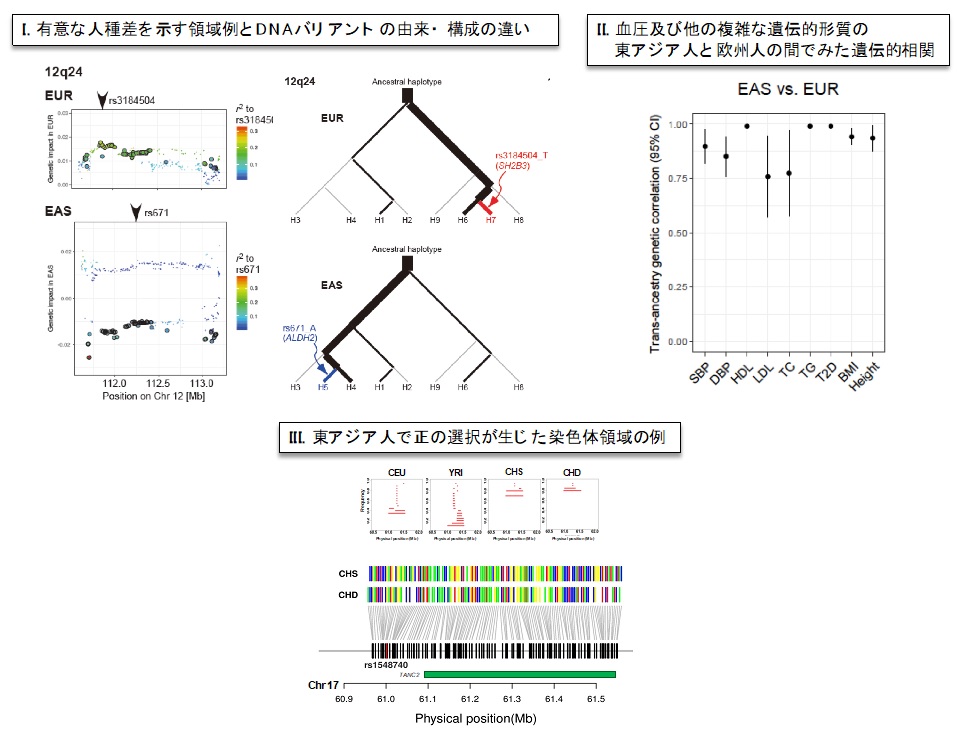 我々は、こうした状況を踏まえつつ、大規模なGWASデータをもとに、東アジア人と欧州人の間での、血圧関連遺伝子座のDNAバリアントの由来・構成の違いと自然選択の影響を実証して「祖先特有バリアントの遺伝的関連モデル」を新たに提唱しました。
我々は、こうした状況を踏まえつつ、大規模なGWASデータをもとに、東アジア人と欧州人の間での、血圧関連遺伝子座のDNAバリアントの由来・構成の違いと自然選択の影響を実証して「祖先特有バリアントの遺伝的関連モデル」を新たに提唱しました。
総括と展望
次世代シーケンサーをはじめとするゲノム解析技術の進歩とともに、高血圧などの複雑な遺伝的性質—多因子疾患—の成因探究も分子レベルで取り組まれる段階になってきました。高血圧などの多因子疾患の人種差は、心血管系合併症の起こり易さの違いだけでなく、治療薬の効果の違いなどにも認められており、人種差の原因を分子レベルで明らかにすることは広く臨床的対応の精密化—プレシジョン・メディシン—に関わります。疾患感受性遺伝子の数は極めて多く、食事、嗜好品、気候など様々な環境要因との複雑な相互作用が推測されていることからも、全容解明は容易でありません。しかし自然選択が高血圧などの多因子疾患の成因に影響しているという本研究の知見は、従来からの仮説を一歩前進させ、メカニズムの解明と予測・診断法の開発に大きなインパクトを与えるものです。
用語の説明
- ゲノムワイド関連解析:特定の集団において、ある遺伝的バリエーション(多型)が、注目する病気の表現型と関連するか否かを検証するのが関連解析(association study)である。ここでいうところの表現型には量的なもの(血圧値など)と質的なもの(高血圧の有無など)とがあり、前者については集団全体を対象とし、後者については(集団の一部である)case群とcontrol群の間の比較により、統計学的有意性を調べる。ゲノムスキャンでは、全く仮説をたてずに「探索する」ため、従来は知られていなかったパスウェイに関わる遺伝子を同定できる可能性がある。ただし、遺伝的効果が比較的マイルドな、高血圧等の多因子疾患のゲノムスキャンにおいて、成否の鍵を握るのは、サンプルサイズ、及びゲノムワイドな多型(特にSNP)情報の網羅性である。ヒトゲノムは32億塩基対から成り、そこに1500万箇所以上のSNPsが存在すると推定されている。これら全てのSNPsを一人ひとり調べることは大変な作業であるが、標識SNPs(遺伝子多型のロードマップの役割を果たすDNA配列の一部分)を中心に調べることで省力化、低コスト化が可能となる。このように絞り込んだ数十万以上のSNPsを代表セットとして遺伝型決定することで、計算上は、全ゲノムのバリエーションの約90%をカバーできる。
- ゲノムワイドな有意水準:膨大な数のSNPのなかから「真の」関連を見出すためには、繰り返し検証する(再現性を確認する)ことで統計学的なノイズ(偽陽性)を除く必要がある。また上述した1500万箇所以上のSNPsどうしには連鎖不平衡が存在するため、約100万種類の独立した検定を繰り返したと想定し、多重検定補正のされたp値 0.05 ÷ 100万 = 5×10-8がゲノムワイドな有意水準として一般に採用されている。
- 集団遺伝学:生物の遺伝現象を、一人ひとりの個体でなく集団について研究する遺伝学の一分野であり、集団の遺伝的構造を支配する法則、同構造が変化するプロセス、または変化してきた過去を再現するための方法などを研究する。
- 精密マッピング:GWAS及びそのメタアナリシスで見出された遺伝子座は、疾患感受性遺伝子そのものを明示しているわけではない。最も強い遺伝的関連を示すバリアントは、必ずしも、特定遺伝子のタンパク・コード配列や、従来注目されてきた発現調節領域に位置するわけでなく、しばしば近傍の遺伝子から数十、数百kb離れていたり、大きなイントロンの真ん中に位置していたりする。それゆえ様々な生物情報学的手法・データを組み合わせることにより、遺伝子座の原因バリアントや疾患感受性遺伝子を絞り込む作業を精密マッピングという。
- ハプロタイプ:両親から一本ずつ同種の染色体を受け継ぎ、一対の相同染色体が生成されるが、そのどちらか一方の染色体(ハプロイド)に存在する遺伝的バリアントのアレル(対立遺伝子)の組み合わせをハプロタイプとよぶ。
- 倹約遺伝子仮説:現代社会で肥満や2型糖尿病が増えている理由を説明するために提唱された仮説の一つである。太古の環境では食物を安定的に確保できる保証がなく、食物を摂取できるときに体内に脂肪としてエネルギーを貯め込める体質が生存にとって有利であったが、食物が豊富な現代の環境では、そうした体質が肥満や2型糖尿病の原因になったという仮説が1962年に提唱された。同仮説には反論も少なからずあり、確定的な証拠はまだ得られていない。
発表雑誌
雑誌名:Nature Communications
論文名:Interethnic analyses of blood pressure loci in populations of East Asian and European descent
参照URL
Nature Communications
(https://www.nature.com/ncomms/)
本件に関するお問合せ先
国立国際医療研究センター研究所 遺伝子診断治療開発研究部
部長 加藤 規弘 (かとう のりひろ)
電話:03-3202-7181(内線2896)
FAX:03-3202-7364
E-mail:nokato@ri.ncgm.go.jp
〒162-8655 東京都新宿区戸山1-21-1
取材に関するお問合せ先
国立国際医療研究センター 企画戦略局 広報企画室
広報係長:西澤 樹生(にしざわ たつき)
電話:03-3202-7181(代表) <9:00~17:00>
E-mail:press@hosp.ncgm.go.jp















